エンパグリフロジンは2型糖尿病患者の心血管イベントを抑制できますか?実はオープンラベルですか?(EMPA-REG OUTCOME: NEJM.2015 Free)
Empagliflozin, Cardiovascular Outcomes, and Mortality in Type 2 Diabetes.
Zinman B et al.; EMPA-REG OUTCOME Investigators.
N Engl J Med. 2015 Nov 26;373(22):2117-28.
www.ncbi.nlm.nih.govPMID: 26378978
ClinicalTrials.gov No.: NCT01131676
【資金提供】
ベーリンガー・インゲルハイムBoehringer Ingelheim
イーライ・リリーEli Lilly
【利益相反COI or 開示disclosure】
めっちゃある(本文参照)。個人的には "The trial was designed and overseen by a steering committee that included academic investigators and employees of Boehringer Ingelheim." という部分がかなり気になる。
⌘ 結論
標準治療へのエンパグリフロジン追加はハイリスク 2型糖尿病患者における心血管死を抑制した。
ただしブラインドが破綻している可能性と奇妙な試験結果、患者背景から日本人への外挿は慎重に行う必要があると考えられる。
→2017.5.16追記
⌘ 私的背景
先日 EBM勉強会に参加し本論文を読んだ。その中で気になった点がいくつかあったので再度、批判的吟味しつつ考えをまとめてみる。
⌘ RobotReviewerによる Risk of Bias Table

⌘ PICOT
P: 18歳以上の 2型糖尿病患者 7020例。心血管疾患の既往歴あり
(組入れ基準:BMI 45以下, eGFR 30 mL/min/1.73m2以上, ランダム化前の 12週間血糖降下薬を飲んでいない状態でHbA1c 7.0~9.0%,あるいは血糖降下療法を受けている安定した状態で HbA1cが 7.0~10.0%。
除外基準:早朝空腹時血糖 240mg/dL以上、肝疾患、組入れ前 3ヶ月以内に心臓手術や血行再建術が予定されている患者、eGFR 30 ml/min/1.73m2未満、減量手術、血液疾患、癌の既往歴、本薬を含め治療薬使用が禁忌の患者、抗肥満薬使用、全身性のステロイド使用、甲状腺ホルモンのタイトレーションを行っている患者、状態が不安定な内分泌疾患を有す患者、妊婦・授乳婦、アルコール依存・薬物依存、他臨床研究に参加中の患者、臨床的症状不良な患者、急性冠症候群・脳卒中・一過性脳虚血発作を有す患者)
I : 標準治療へのエンパグリフロジン(商品名:ジャディアンス)10 mg あるいは 25 mg
C: 標準治療へのプラセボ追加
O: primary --- 3-point MACE
(心血管死、無症候性心筋梗塞を除く非致死性心筋梗塞、非致死性脳卒中)
key secondary --- primary outcome + 不安定狭心症による入院
T : ランダム化比較試験、プラセボ対照、非劣性試験(FDA勧告に従いマージン1.3)、
優越性についても検討(マージン1.0?記載無し)、追跡期間は中央値 3.1年(治療期間は 2.6年)
⌘ ランダム割り付けされているか?(観察者バイアスはないか?)
→されている。IVRS(Interactive Voice Response System)および Interactive Web Response System(IWRS)を採用。
→層別割り付けを実施。
HbA1c:8.5%未満、8.5%以上
BMI :30未満、30以上
eGFR :30~59、60~89、90以上(ml/min/1.73m2)
居住地 :北米(+オーストラリア+ニュージーランド)、ラテンアメリカ、ヨーロッパ、アフリカ、アジア
⌘ ブラインドされているか?(マスキングにより観察者バイアスは抑えられているか?)
→一応されている。破綻している可能性については後述。ハードエンドポイントだからそこまで影響無いかもしれない。
⌘ 隠蔽化されているか?(選択バイアスはないか?)
→されていると判断。中央割り付けであるため。
⌘ プライマリーアウトカムは真か?明確か?
→真であると判断した。ただし複合エンドポイントである点を考慮する必要がある。
⌘ 交絡因子は網羅的に検討されているか?
→概ねされていると判断した。CRPや BNPがあっても良いかも。
あとウエストサイズ。←あかん。これはエビデンスなかった(2017.5.16追記)。
⌘ Baseline は同等か?
→概ね同等であると判断した(Appendix Table S2参照)。
⌘ ITT 解析されているか?
→改変 ITT解析。最初は 7028例だったが、結果は 7,020例の解析だった。Full Analysis Set(FAS)である。
⌘ 追跡率(脱落)はどのくらいか?結果を覆す程か?
→FASだとほぼ100%(99.89%)。一応、脱落率を算出すると、2割を超える(追跡率 8割を切っている)ので脱落が多い気はする。リアルワールドではこのぐらいなのかな?非劣性試験のため Per Protocol Analysis(PPA)との比較も重要だが、この程度の脱落ならば差はなさそうである。
5,029 / 7,020 =71.6%(Appendix Figure S1より計算)
⌘ サンプルサイズは充分か?
→ 691と計算されており、primary outcomeは 772例と症例数も充分(多過ぎ?)。
⌘ 結果は?
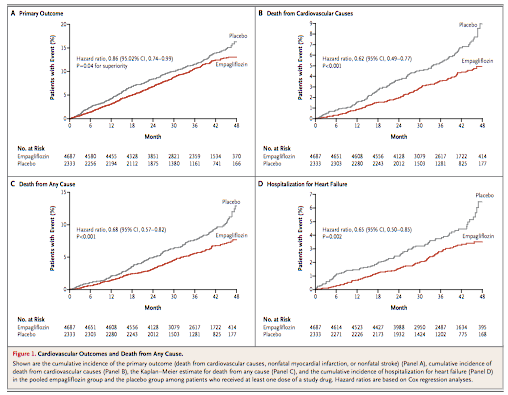
(Figure 1:本文より引用)
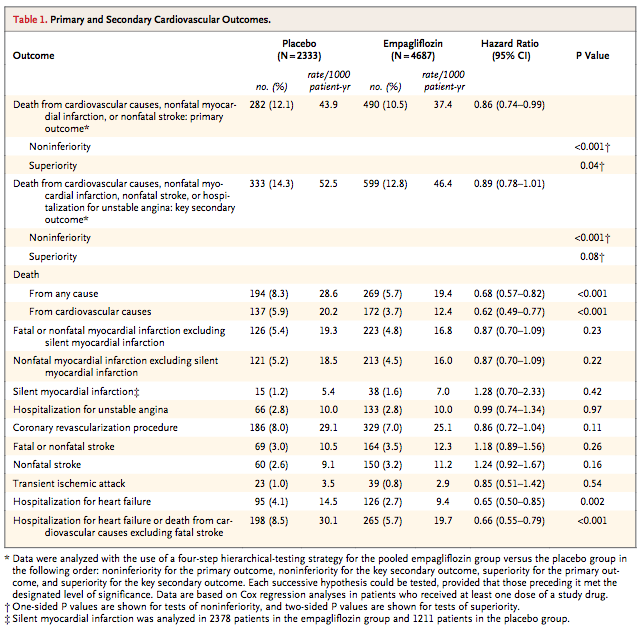
(Table 1:本文より引用)
→ Primary Endpoint(標準治療への追加効果)
エンパグリフロジン群(10 mg + 25 mgのプール):10.5%
プラセボ群 :12.1%
HR =0.86(95%CI =0.74〜0.99)
非劣性(両側;マージン1.3) :P <0.001
優越性(片側;マージン不明):P =0.04
RR =0.87
RRR =0.13(13%)
ARR =1.6%
NNT =63人
→ Key Secondary Endpoint
エンパグリフロジン群(10 mg + 25 mgのプール):12.8%
プラセボ群 :14.3%
HR =0.89(95%CI =0.78〜1.01)
非劣性(両側;マージン1.3) :P <0.001
優越性(片側;マージン不明):P =0.08 有意差無し
--- その他のアウトカム ---
→全死亡
エンパグリフロジン群(10 mg + 25 mgのプール):5.7%
プラセボ群 :8.3%
HR =0.68(95%CI =0.57〜0.82) P <0.001
→心血管死
エンパグリフロジン群(10 mg + 25 mgのプール):3.7%
プラセボ群 :5.9%
HR =0.62(95%CI =0.49〜0.77) P <0.001
エンパグリフロジン群(10 mg + 25 mgのプール):4.8%
プラセボ群 :5.4%
HR =0.87(95%CI =0.70〜1.09) P =0.23
→無症候性心筋梗塞
エンパグリフロジン群(10 mg + 25 mgのプール):4.5%
プラセボ群 :5.2%
HR =1.28(95%CI =0.70〜2.33) P =0.42
→不安定狭心症による入院
エンパグリフロジン群(10 mg + 25 mgのプール):2.8%
プラセボ群 :2.8%
HR =0.99(95%CI =0.74〜1.34) P =0.97
→冠動脈血管再建術
エンパグリフロジン群(10 mg + 25 mgのプール):7.0%
プラセボ群 :8.0%
HR =0.86(95%CI =0.72〜1.04) P =0.11
→致死性 or 非致死性脳卒中
エンパグリフロジン群(10 mg + 25 mgのプール):3.5%
プラセボ群 :3.0%
HR =1.18(95%CI =0.89〜1.56) P =0.26
→非致死性脳卒中
エンパグリフロジン群(10 mg + 25 mgのプール):3.2%
プラセボ群:2.6%
HR =1.24(95%CI =0.92〜1.67) P =0.16
→一過性脳虚血発作(TIA)
エンパグリフロジン群(10 mg + 25 mgのプール):0.8%
プラセボ群:1.0%
HR =0.85(95%CI =0.51〜1.42) P =0.54
→心不全による入院
エンパグリフロジン群(10 mg + 25 mgのプール):2.7%
プラセボ群 :4.1%
HR =0.65(95%CI =0.50〜0.85) P =0.002
エンパグリフロジン群(10 mg + 25 mgのプール):5.7%
プラセボ群:8.5%
HR =0.66(95%CI =0.55〜0.79) P <0.001
⌘ 考察
観察期間は約 3年であり、心血管イベントを抑制するには少し短いという印象。事実、DPP-4阻害薬であるシタグリプチン(商品名:ジャヌビア / グラクティブ)の大規模臨床試験TECOS(PMID:26052984)では、観察期間 3年(中央値)でプラセボ群に対して非劣性までしか示せていない(プラセボの非劣性って、もう経過観察で良くないですか?)。しかしエンパグリフロジンは、たった 3年?でプライマリーアウトカムに対し非劣性だけでなく優越性も示した(あくまで非劣性試験であり優越性については両側マージンを設定し、再度試験する必要があるがコストかかる。マージン1.0?も妥当と言って良いかどうか疑問)。DPP-4阻害薬の大規模臨床試験については患者背景が異なるという指摘もある。低血糖症状を引き起こさないようハイリスク患者は除外されているため効果を拾えていないという主張。この議論については次回以降ブログで取り上げたい。
メトホルミン(商品名:メトグルコ)以来の心血管イベント抑制は非常にインパクトがあり、臨床的にも有益な結果であると考えられる。しかし標準治療の上乗せ、add-onによる効果であることには留意する必要がある。つまり 2型糖尿病の治療戦略において、エンパグリフロジンが血管合併症予防のファーストラインにはならないということ。過度の飲酒や腎機能が過度に低下していない症例に対しては、まずメトホルミンを最大用量まで増量してから、エンパグリフロジン追加について患者と shared decision making しても良いのではないでしょうか(もちろん乳酸アシドーシスについては注意深く経過観察する)。
また SGLT2阻害薬カナグリフロジンの臨床試験 Canagliflozin Cardiovascular Assessment Study (CANVAS) trialの中間解析で "下肢切断リスク上昇の可能性" が示唆されており、FDAから安全性情報が発出されています(下記サイト内より抜粋)。従って 現時点で SGLT2阻害薬は、糖尿病治療のセカンドライン、サードラインにも成り得ないのではないかなと個人的には考えています(患者背景にもよりますが)。
心血管疾患の既往歴を有すハイリスク 2型糖尿病患者においては、血圧や脂質コントロールが心血管疾患の予防に重要ではないか、との意見もある(PMID:23992603)。血糖コントロールの指標である HbA1cについては、下げ過ぎはむしろ害となることが ACCORD試験(PMID:18539917)をはじめ相次いで報告されている。今一度「必要な患者に、必要な薬を、必要な用量、必要な期間」、使用するということに対して各々が考え、向き合う必要があるのではないでしょうか。
-------
⌘ 考察その 2
本試験あるいは他の報告で気になった点を以下に考察していこうと思う。
①ブラインドは破綻していた?
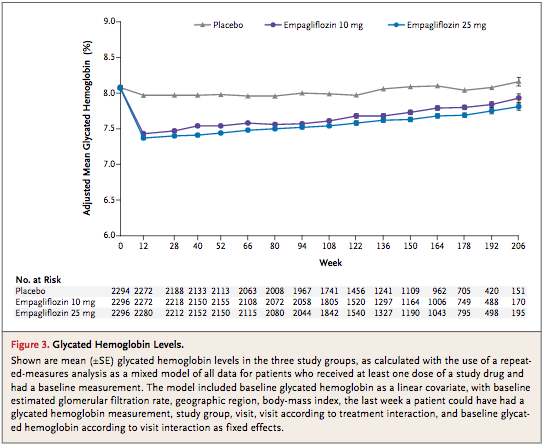
(Figure 3:本文より引用)
本試験は 42ヶ国、590施設で実施された。Figure 3の結果から投与 3ヶ月後にはエンパグリフロジン群で HbA1cが 0.7%程度低下している。プラセボ群が 0.1〜0.2%ぐらいの下がり幅であるため、一部の施設でブラインドは破綻していたのではないでしょうか。そうするとエンパグリフロジン群で心不全による入院が有意に低下しているのも納得がいく。ただブラインドであろうと無かろうと全死亡・心血管死というハードエンドポイントに有意な差があるため、本試験結果は妥当であると考えられる。ここで言いたいことは PROBE法でハードエンドポイントだけ見ればコストカットできたのではないかということ。
②心血管死の減少は心不全の抑制?それとも。。。
勉強会参加時にも話にあがりましたが、はたしてエンパグリフロジンの全死亡リスク低下はどのようにもたらされているのでしょうか? 2016年に発表された "サブグループ解析" 論文(PMID;26819227)において、ベースライン時の心不全の有無とは関係なくエンパグリフロジンが心血管死および心不全による入院を減少させた可能性が示唆されています。サブグループ解析であるため、あくまで "仮説生成" ですがエンパグリフロジンの心血管イベント抑制効果は心不全の増悪抑制ではない可能性が考えられます。これはメイン論文の Table S5をみても分かります(以下参照)。モヤモヤする。
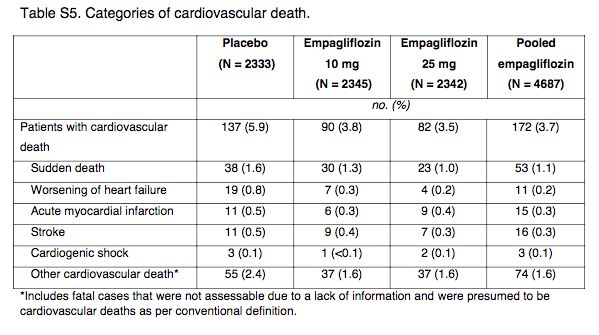
(Table S5:Supplementary Appendix より引用)
各エンドポイントの絶対差
→ 突然死 =0.4%
→ 心不全の増悪 =0.6%
→ 急性心筋梗塞 =0.2%
→ 脳卒中 =0.2%
→ 心原性ショック =0.0%
→ 他の心血管死 =0.8%(イベント数でみるとこれが多い)
③作用機序の一部は利尿薬と同じ?
面白いアプローチでエンパグリフロジンの心血管イベント抑制効果を説明しようとしている研究者もいます。本論文(PMID:27291329)では、エンパグリフロジンの心血管への有益な効果は尿中への糖排出ではなく、これに伴う利尿作用によるものではないかという仮説に基づき文献検索を行ったナラティブレビュー。結果はよく分からんとのこと。新しい知見を待っているようです。
④10 mgと 25 mgをプールして解析したのはなぜか?
不明だが、デザイン論文にも 2群プールして解析する旨が記載されているため、キーオープンしてから解析方法を変えたわけではない。
メリットとしては、試験実施側が informed consentを患者から取りやすくなる、患者側は1/2(50%)よりも 2/3(66.7%)、つまり絶対差で 16.7%試験薬に割り付けられる可能性が増えるため、ある種 Win-Win の関係と言えるだろう。
(閑話休題:個人的には臨床試験を人体実験と捉えているため、"新しかろう良かろう" という風潮には違和感を覚える。薬はベネフィットだけではなく必ずリスクが伴うことも伝えていきたい。しかし、そんなこと言ってたら新薬開発は進まない。新薬により恩恵を受ける患者がいることも重々理解しているつもりである。例えば近年、急速に市場を拡大しているC型肝炎治療薬は、間違えなくリスクよりベネフィットが優っている。C型肝炎から肝硬変、肝がんへの移行、これに伴う治療費、治療期間を考慮しても、やはり使う方が良いという結論に達した)
プラセボ群、試験薬群を 1: 2で割り付けるデザインの亜型?と捉えても良いかもしれない。従って、10 mg群、25 mg群で各々、プラセボと比べ有意差が出なかったのも納得できる。単純にサンプル数が足りないのだ。
ただし、プライマリーエンドポイントのイベント数が多過ぎる点は気にかかる。実際は 772例と、サンプルサイズ 691例よりもかなり多い。プライマリーエンドポイントの 95%信頼区間は 0.74〜0.99であり、症例数が少なくなったとしても非劣性マージン 1.3をまたがなかったかもしれない。しかし優越性は認められなかったかもしれない。←またまた勘違い。非劣性試験なので症例数は多い方が良く、少なければ少ない程、非劣性を達成しやすい。脱落が多い場合も非劣性を証明しやすいため、この場合は ITT解析と Per Protocol 解析との比較が重要となる。つまり本試験の症例数は充分である。しかし優越性についてはどうだろうか?(2015.5.16追記)
モヤモヤしつつ以上としたい。